Telah kita pelajari tentang pengertan termokimia pada postingan sebelumnya. Bahwa Termokimia adalah cabang ilmu kimia yang mempelajari tentang perubahan kalor atau energi yang menyertai suatu reaksi kimia, baik yang diserap maupun yang dilepaskan. Untuk lebih lengkap nya.

Dibawah ini admin sajikan beberapa contoh soal dan pembahasannya tentang materi termokimia.
Soal No.1
Diketahui 1 mol NO terurai menjadi unsur-unsur pembentuknya dengan melepaskan kalor sebesar 90,4 kJ.
a. Tuliskan persamaan termokimia dari reaksi tersebut!
b. Gambarkan diagram tingkat energinya!
c. Tentukan perubahan entalpi untuk reaksi pembentukan 1,5 mol zat tersebut dan persamaan termokimianya!
Pembahasan:
a. Reaksi penguraian NO melepaskan kalor. Dengan demikian, perubahan entalpinya berharga negatif. Persamaan termokimia untuk 1 mol NO sebagai berikut.
NO(g) → ⅟2 N2(g) + ⅟2 O2(g) ∆H = -90,4 kJ/mol
b. Diagram tingkat energinya:
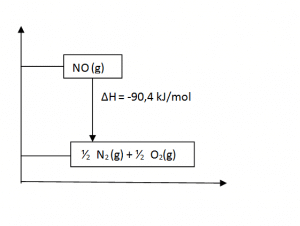
c. Perubahan entalpi pembentukan untuk 1,5 mol NO sebagai berikut.
Reaksi pengurai:
NO(g) → ⅟2 N2(g) + ⅟2 O2(g) ∆H = -90,4 kJ/mol
Reaksi pembentukan:
NO(g) → ⅟2 N2(g) + ⅟2 O2(g) ∆H = -90,4 kJ/mol
untuk 1,5 mol NO perubahan entalpinya sebesar 1,5 x 90,4 kJ = 135,6 kJ.
Jadi, persamaan termokimia untuk pem-bentukan 1,5 mol NO sebagai berikut.
N2(g) + O2(g) → 2NO(g) ∆H = + 135,6 kJ
Soal No.2
Kelompokkan reaksi-reaksi di bawah ini ke dalam reaksi endoterm atau reaksi eksoterm!
a. N204 (g) → 2N02(g) ∆H = +58 kJ
b. N2(g) + 3H2(g) → 2NH3(g) ∆H = -92 kJ
c. HCI(aq) + NaOH(aq) → NaCI(aq) + H20(ℓ) ∆H = -56 kJ
d. 2C(s) + H2(g) → C2H2(g) ∆H = +225 kJ
Pembahasan:
Reaksi:
- 2C(s) + H2(g) → C2H2(g) ∆H = +225kJ
- N204(g) → 2NO2(g) ∆H = +58 kJ
Termasuk reaksi endoterm karena memiliki ∆H positif. Sementara itu, reaksi:
- HCI(aq) + NaOH(aq) → NaCI(aq) + H20(ℓ) ∆H = -56 kJ
- N2(g) + 3H2(g) → 2NH3(g) ∆H = -92kJ
Termasuk reaksi eksoterm karena memiliki AH negatif.
Soal No.3
Diketahui entalpi pembentukan 14 g gas etilena (C2H4) adalah +26,15kJ.
a. Berapakah besarnya kalor yang dilepaskan untuk menguraikan 84 g gas etilena menjadi unsur-unsurnya?
b. Tuliskan persamaan termokimianya!
Pembahasan:
Perbandingan koefisien = perbandingan mol

Soal No.4
Diketahui persamaan termokimia reaksi pembakar- an gas asetilen (C2H2) sebagai berikut.
2C2H2(g) + 502(g) → 4C02(g) + 2H20(ℓ)
∆H = -2.599,1 kJ.
a. Tentukan entalpi pembakaran standar gas asetilen!
b. Hitung kalor yang dihasilkan pada pembakaran 10 L gas asetilen!
Pembahasan:
a. Entalpi pembakaran standar gas asetilen sebagai berikut.
Reaksi pembakaran pada persamaan reaksi 2C2H2 + 5O2 -+ 4CO2+ 2H2O menunjukkan bahwa pembakaran tersebut dilakukan untuk 2 mol gas C2H2, dengan membebaskan kalor sebesar 2.599,1 kJ. Oleh karena itu, entalpi pembakaran standar gas asetilen harus ditentukan untuk 1 mol gas asetilen. Dengan demikian, besarnya entalpi pembakaran standar gas asetilen adalah 2.599,1 kJ : 2 = 1.299,6 kJ.
b.Besarnya kalor yang dihasilkan pada pem-bakaran 10 L gas asetilen sebagai berikut. mol gas asetilen pada kondisi standar:

Soal No.5
Diketahui entalpi pembentukan standar (∆H°f) H20(ℓ) = -285,85 kJ/mol. Berapakah kalor yang diperlukan untuk menguraikan 13 gram air menjadi hidrogen dan oksigen pada keadaan standar? (Ar H = 1, Ar O = 16)
Pembahasan:
AH°f H20(ℓ) = -285,85 kJ/mol
Persamaan termokimia reaksi pembentukan H20:
H2(g) + ⅟2 O2(g) →H20(ℓ) ∆H = -285,85 kJ/mol.
Persamaan termokimia reaksi penguraian H20(ℓ)
H20(ℓ) →H2(g) + ⅟2 O2(g) ∆H =+285,85 kJ/mol.
Jumlah mol air dalam 10 gram air = 13 g /18g/mol – 0,72 mol.
Kalor yang diperlukan untuk menguraikan 13 g air = 0,72 mol/ 1 mol x 285,85 kJ/mol = 205,812 kJ/mol
Jadi, kalor yang diperlukan untuk menguraikan 13 gram air menjadi hidrogen dan oksigen sebesar 205,812 kJ.
Artikel Paling Populer :
- Makromolekul : Protein Kali ini kami akan membahas materi kimia tentang asam amino pada makromolekul. Protein Merupakan polimer alam yang tersusun dari asam-asam amino melalui ikatan peptida, sehingga protein juga disebut sebagai polipeptida.…
- Pengertian, Rumus dan Contoh Soal Molalitas dan… Pengertian, Rumus dan Contoh Soal Molalitas dan Fraksi Mol Lengkap – Molalitas atau kosentrasi molal adalah ukuran konsentrasi dari suatu zat terlarut di dalam suatu larutan dalam hal jumlah zat dalam…
- Pengertian, Cara Menentukan, Contoh Soal Rumus… Pengertian, Cara Menentukan, Contoh Soal Rumus Empiris dan Rumus Molekul Senyawa Lengkap – Rumus kimia merupakan salah satu ciri khas dari senyawa kimia. Rumus kimia terbagi menjadi 2 (dua) yaitu rumus…
- Penjelasan Lengkap tentang Katabolisme, Pengertian… Penjelasan Lengkap tentang Katabolisme, Pengertian dan Jenis Katabolisme Melanjutkan postingan sebelumnya seputar anabolisme dan enzim. Kali ini kita akan bahas tuntas mengenai katabolisme. Simak uraian berikut ini. Sebelum diserap oleh…
- Penyelesaian PLSV dengan Persamaan-Persamaan yang Ekuivalen Sebelumnya kami sudah dibahas tentang cara penyelesain persamaan linear satu variabel dengan cara substitusi (penggantian). Cara itu kelihatan agak ribet karena harus mencoba satu persatu suatu bilangan yang jumlahnya tidak terhingga.…
- Menyelesaikan Masalah Dengan Menggunakan Konsep Himpunan Jika Anda amati masalah dalam kehidupan sehari-hari maka banyak di antaranya dapat diselesaikan dengan konsep himpunan. Agar dapat menyelesaikannya, Anda harus memahami kembali mengenai konsep diagram Venn dan Anda harus dapat menyatakan permasalahan…
- Reaksi Kesetimbangan Kimia Dalam Industri Dan… Berdasarkan azas Le Chatelier pada artikel sebelumnya, diketahui bahwa sistem yang berada dalam kesetimbangan akan selalu berusaha untuk mempertahankan kesetimbangannya. Dengan demikian, apabila terjadi aksi maka sistem akan mengalami pergeseran agar kesetimbangan tercapai…
- Jenis Jenis Hubungan Kuantitatif Antara Pereaksi dan… Guldberg dan Waage mengemukakan hukum kesetimbangan dalam reaksi kesetimbangan kimia sebagai berikut. ”Dalam keadaan setimbang pada suhu tertentu, hasil kali konsentrasi hasil reaksi dibagi hasil kali konsentrasi pereaksi yang ada dalam sistem kesetimbangan…
- Rumus Barisan Dan Deret Aritmatika Beserta Contoh… Rumus Barisan Dan Deret Aritmatika Beserta Contoh Soal Dan Penyelesaian Lengkap – Aritmatika atau Aritmetika berasal dari bahasa yunani αριθμός yang berarti angka yang dulu biasa disebut dengan Ilmu Hitung yaitu cabang tertua atau pendahulu…
- Hidrolisis Garam : Pengertian, Macam, Dan Rumus,… Karena pada kesempatan kali ini disini akan mengulas tentang pengertian Hidrolisis Garam, macam Hidrolisis Garam, dan rumus Hidrolisis Garam beserta contoh soalnya secara lengkap. Oleh karena itu marilah simak ulasan…
- Pengertian dan Cara Menghitung Kemolaran, Kemolalan… Pengertian dan Cara Menghitung Kemolaran, Kemolalan dan Kenormalan Larutan Lengkap – Molaritas adalah jumlah mol zat terlarut dalam 1 liter larutan atau 1 mmol zat terlarut dalam 1 ml larutan. Satuan…
- Pengertian Teori Tumbukan dan Faktor-Faktor yang… Reaksi kimia terjadi ketika partikel-partikel zat yang bereaksi (pereaksi) saling bertumbukan. Namun, tidak semua tumbukan yang terjadi akan menghasilkan zat baru. Zat baru dapat dihasilkan dari tumbukan yang berlangsung sempurna.…
- Himpunan Penyelesaian Persamaan Linear Satu Variabel Sebelumnya sudah dibahas bahwa kalimat terbuka yang dihubungkan oleh tanda sama dengan (=) disebut persamaan, sedangkan persamaan dengan satu variabel berpangkat satu atau berderajat satu disebut persamaan linear satu variabel. Bagaimana cara menentukan…
- Laju Reaksi Apa Itu Laju Reaksi? Jadi laju reaksi itu adalah ya, laju dari sebuah reaksi. Bagaimana pengurangan suatu konsentrasi pereaksi atau penambahan konsentrasi. Satuannya adalah mol dm-3 atau M s-1 Pengurangan…
- PENYETARAAN REAKSI REDOKS Dua metode yang bisa digunakan adalah metode bilangan oksidasi dan setengah reaksi Metode bilangan oksidasi Langkah-langkah menyetarakan reaksi redoks dalam suasana asam Tentukan reaksi oksidasi dan reduksi dengan cara menuliskan perubahan…
- Termokimia – Pengertian, Reaksi Termokimia dan… Termokimia adalah cabang ilmu kimia yang mempelajari tentang perubahan kalor atau energi yang menyertai suatu reaksi kimia, baik yang diserap maupun yang dilepaskan. Hukum kekekalan energi menyatakan bahwa energi tidak…
- Apa Pengertian Senyawa Mungkin kalian bingung dengan pengertian dari senyawa dan molekul. Apakah senyawa dan molekul memiliki definisi yang berbeda atau sama? Baiklah kita sekarang akan bahas terlebih dahulu tentang senyawa. Senyawa adalah zat yang…
- Termokimia Jadi termokimia apa sih? kita bakal ngebahas tentang sistem dan lingkungan, yuk langsung saja! Perubahan Entalpi Entalpi sendiri itu delta H, jadi perubahan energi pada suatu zat Ada dua jenis:…
- Cara Membuat / Menggambar Diagram Venn Jika Anda mempelajari konsep himpunan maka Anda akan mengenal sub materi tentang Diagram Venn atau diagram gambar. Apa itu pengertian diagram ven? Pengertian Diagram Venn Cara yang memudahkan kita untuk…
- Pengertian dan Contoh Perubahan kimia Perubahan pada zat dibedakan menjadi dua yaitu perubahan fisika dan perubahan kimia. Untuk perubahan secara fisika sudah dibahas pada postingan sebelumnya yang berjudul "perubahan fisika". Pada postingan ini hanya dibahas mengenai perubahan…



