Pernahkah Anda melihat pohon asam jawa? Buah asam jawa tumbuh bergelantung dengan beberapa biji dalam setiap buahnya. Beberapa kandunga asam jawa berupa senyawa asam seperti asam sitrat, asam tartart, asam suksinat, asam malat dan asam asetat. Kandungan kimia asam jawa berkhasiat untuk mengobati asma, batuk, demam dan bengkak karena sengatan lipan atau lebah. Apakah yang dimaksud dengan senyawa asam? Temukan jawabannya pada uraian dibawah ini..
Konsep Asam-Basa
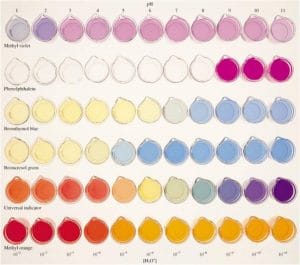
Istilah asam (acid) berasal dari bahasa latin acelum yang berarti cuka. Sebaliknya, senyawa yang memiliki sifat sangat berbeda dibanding asam yaitu senyawa alkali (basa) yang diturunkan dari abu berbagai tanaman, Suatu senyawa dapat diketahui bersifat asam atau basa jika berada dalam bentuk larutannya. Istilah asam digunakan untuk senyawa yang dalam bentuk larutannya menghasilkan ion hidrogen (H+). Sementara itu, basa digunakan untuk senyawa yang dalam bentuk larutannya terurai menjadi ion hidroksida (OH-).
Teori Arrhenius
Pada tahun 1886, Svante August Arrhenius, ilmuwan dari Swedia menyatakan teori tentang asam dan basa. Menurut Arrhenius, asam merupakan zat yang menghasilkan ion hidrogen (H+) apabila terlarut dalam air, sedangkan basa didefinisikan sebagai zat yang menghasilkan ion hidroksida (OH-) jika dilarutkan dalam air. Jadi, teori ini hanya terbatas pada pelarut air saja. Jika pelarutnya bukan air dan zat yang terurai tidak mengandung H+ dan OH-, teori ini tidak berlaku. Contoh reaksi yang tidak dapat dijelaskan dengan teori Arrhenius:
NH3(g) + HCIfg) NH4CI(s)
Reaksi tersebut tidak melibatkan adanya H+ dan OH-. Proses terurainya zat menjadi ion-ion disebut ionisasi.
Beberapa contoh ionisasi asam dan basa sebagai berikut.
Reaksi ionisasi pada beberapa asam:
HNO3 → H+ + NO3
H2SO4 → 2H+ + SO24-
H3PO4 → 3H+ + PO34-
H2C2O4 → 2H+ + C2O24-
Reaksi ionisasi pada beberapa basa:
KOH → K+ + OH-
Ca(OH)2 → Ca2+ + 20H-
Ba(OH)2 → Ba2+ + 20H-
Reaksi-reaksi yang tidak melibatkan H+ dan OH- dapat dijelaskan menggunakan teori Bronsted-Lowry dan teori Lewis.
Berdasarkan jumlah ion H+ (untuk asam) dan ion OH- (untuk basa) yang dihasilkan dalam reaksi ionisasi, senyawa asam-basa dapat dikelompokkan menjadi asam-basa monoprotik (jumlah ion H+/OH¬- > 1) dan asam-basa poliprotik (jumlah ion H+/OH¬- > 1) Asam-basa poliprotik dapat mengalami beberapa kali reaksi ionisasi. Perhatikan contoh berikut.
Contoh :
H3PO4(aq) 3H+(aq) + PO34-(aq)
Reaksi ionisasi 1 = H3PO4(aq) → H+(aq) + H2PO-(aq)
Reaksi ionisasi 2 = H2PO-4(aq) → H+(aq) + HPO24-(aq)
Reaksi ionisasi 3 = HPO24-(aq) → H+(aq) + PO34- (aq)
Teori Bronsted-Lowry
Pada tahun 1923, Johannes Nicolaus Bronsted, kimiawan dari Denmark dan Thomas Martin Lowry, kimiawan dari Amerika Serikat mendefinisikantentang asam-basa. Menurut Bronsted-Lowry, asam adalah spesi yang memberikan (donor) proton, sedangkan basa adalah spesi yang bertindak sebagai penerima (akseptor) proton dalam suatu reaksi transfer proton.
Teori Bronsted-Lowry melengkapi konsep asam-basa Arrhenius. Ion hidroksida dalam teori Arrhenius tetap menjadi basa dalam teori Bronsted- Lowry. Ion hidroksida (OH“) ini menerima ion hidrogen (H+) membentuk H20. Pada reaksi asam-basa Bronsted-Lowry terdapat dua pasangan asam-basa konjugasi.
Contoh:
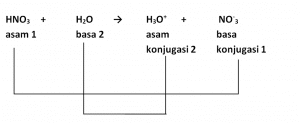
Pada reaksi di atas HNO3 adalah asam karena mendonorkan proton (H+) pada H2O. Sementara itu, H2O merupakan basa karena menerima proton (H+) dari HNO3. Oleh karena itu, H3O+ merupakan asam konjugasi dari H2O dan NO-3 merupakan basa konjugasi dari HNO3.
Teori Lewis
Pada tahun 1923, Gilbert N. Lewis, kimiawan dari Amerika Serikat mendefinisikan asam-basa berdasarkan teori ikatan kimia. Menurut Lewis, asam adalah penerima (akseptor) pasangan elektron bebas. Sementara itu, basa adalah pemberi (donor) pasangan elektron bebas.
Teori asam-basa Lewis lebih luas pengertiannya dibandingkan dengan dua teori sebelumnya. Spesi apa pun yang dapat menerima (akseptor) pasangan elektron bebas disebut asam Lewis. Contoh asam Lewis yaitu H+, B2H6, BF3, AIF3, Fe2+, Cu2+ ,dan Zn2+. Suatu spesi tidak selalu menyediakan orbital kosong untuk menjadi asam Lewis.
Spesi berupa molekul atau ion yang mendonorkan pasangan elektron bebasnya disebut basa Lewis. Contoh ion halida ( Cl-, F-, Br-, dan l-), NH3, OH-, H2O, senyawa yang mengandung unsur N, O, atau S, senyawa golongan eter, keton, dan C02.
Reaksi asam dan basa Lewis sebagai berikut:
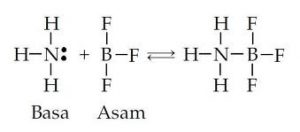
Demikian penjelasan yang bisa kami sampaikan tentang Teori – Teori dan Konsep Asma Basa Menurut Para Ahli Dan Penjelasan. Semoga postingan ini bermanfaat bagi pembaca dan bisa dijadikan sumber literatur untuk mengerjakan tugas. Sampai jumpa pada postingan selanjutnya.
Artikel Paling Populer :
- Unsur, Senyawa dan Campuran Setiap hari kita sering menjumpai benda-benda yang mempunyai suatu bentuk, sifat, dan struktur penyusunnya yang beda-beda. Benda-benda tersebut ada yang dibentuk dari gabungan beberapa benda dan ada pula yang tidak…
- Asam Basa – Mengkaji Dan Mengidentifikasi Sifat… Ketika makan buah jeruk, tentu ada sedikit atau mendominasi rasa masam dari buah jeruk. Rasa masam yang terdapat pada buah jeruk dikarenakan jeruk bersifat asam. Pernahkah Anda memperhatikan kaki atau…
- Makromolekul : Asam Amino Kali ini kami akan membahas materi kimia tentang asam amino pada makromolekul. Asam Amino Asam amino ialah senyawa yang mempunyai gugus asam karbosilat (-COOH) dan gugus amina (-NH2). Rumus umum…
- Asam Basa – Penentuan pH Asam Kuat Dan Basa Kuat… Setelah kita mempelajari tentang pH, pOH, dan pKw, dikatakan bahwa Istilah pH digunakan untuk menyatakan keasaman atau kebasaan suatu larutan. Istilah pH berasal dari potential of hydrogen yang dikemukakan oleh…
- Pengertian Lambung, Bagian, Fungsi dan Penyakit Pada… Pengertian Lambung, Bagian, Fungsi dan Penyakit Pada Lambung Lengkap – Lambung adalah salah satu organ pencernaan pada manusia. Fungsi lambung yaitu untuk menyimpan makanan sementara dan mengolah makanan tersebut agar dapat masuk ke usus kecil.…
- Pengertian Ilmu Kimia Pengertian ilmu kimia, Sejarah, Cabang, Manfaat dan Sifat : Adalah ilmu yang mempelajari tentang komposisi, struktur, sifat dan perubahan dari suatu zat. Pengertian Ilmu Kimia Ilmu Kimia, berasal dari bahasa Arab,…
- Asam Basa – Konsep pH, pOH, dan pKw Pada Larutan Asam Basa Kekuatan asam atau basa suatu larutan dapat ditentukan dari harga pH, pOH, dan pKw larutannya. Istilah pH digunakan untuk menyatakan keasaman atau kebasaan suatu larutan. Istilah pH berasal dari potential…
- Pengertian DNA dan RNA, Fungsi, Struktur dan… Pengertian DNA dan RNA, Fungsi, Struktur dan Jenisnya Terlengkap – Kali ini kita akan membahas tentang DNA (Deoxyribonucleic acid) dan RNA (Ribonucleic acid), serta fungsi, struktur atau komponen penyusun dan jenisnya lengkap.…
- Asam Basa – Menghitung pH Larutan Asam Lemah dan Basa Lemah Asam lemah banyak terdapat dalam buah-buahan seperti mangga, apel, dan jeruk. Asam lemah tidak berbahaya dan boleh dimakan. Basa lemah, seperti aluminium hidroksida (AI(OH)3) dapat ditemukan dalam obat mag. pH…
- Penjelasan Lengkap tentang Katabolisme, Pengertian… Penjelasan Lengkap tentang Katabolisme, Pengertian dan Jenis Katabolisme Melanjutkan postingan sebelumnya seputar anabolisme dan enzim. Kali ini kita akan bahas tuntas mengenai katabolisme. Simak uraian berikut ini. Sebelum diserap oleh…
- Contoh Zat Kimia Sebagai Pengawet Makanan dan Minuman Bahan pengawet adalah bahan kimia yang dapat mencegah atau menghambat proses fermentasi (pembusukan), pengasaman, atau peruraian lain terhadap makanan yang disebabkan oleh mikroorganisme sehingga makanan tidak mudah rusak atau menjadi busuk.…
- Penjelasan Lengkap Konsep Asam Basa Menurut Para Ahli Penjelasan Lengkap Konsep Asam Basa Menurut Para Ahli | Istilah asam (acid) berasalah dari bahsasa latin acelum yang berarti cuka. Sebaliknya,senyawa yang memiliki sifat sangat berbeda disbanding asam yaitu senyawa alkali…
- Definisi dan Contoh Senyawa Terner Pada postingan kali ini akan membahas mengenai senyawa terner. Setelah artikel kami cari di mesin pencarian google tentang senyawa terner, malah kami kebingungan. Ada beberapa blog atau website yang menjelaskan bahwa “senyawa…
- Pengertian Batuan Beku, Proses Pembentukan, Jenis,… Pengertian, Proses Pembentukan, Jenis, Contoh dan Ciri-Ciri Batuan Beku Lengkap – Batuan beku atau batuan igneus merupakan jenis batuan yang terbentuk dari magma yang mendingin dan mengeras dengan atau tanpa…
- Fungsi Larutan Penyangga Dalam Tubuh Dan Kehidupan… Larutan penyangga sangat berperan dalam kehidupan makhluk hidup. Fungsi larutan penyangga dalam tubuh makhluk hidup dan dalam kehidupan sehari-hari sebagai berikut. Fungsi Larutan Penyangga dalam Tubuh Makhluk Hidup pH darah…
- Pengertian Tritrasi,Stoikiometri Larutan Dan Grafik… Titrasi asam-basa merupakan suatu cara yang cukup teliti untuk menentukan konsentrasi suatu asam atau basa. Konsentrasi suatu asam ditentukan dengan cara menitrasi asam dengan basa yang telah diketahui kadarnya, begitu…
- Fungsi Ginjal Dalam Tubuh Manusia dengan Penjelasan… Penjelasan Terlengkap Mengenai Fungsi-Fungsi Ginjal dalam Tubuh Manusia Ginjal merupakan salah satu bagian dari sistem ekkresi pada manusia. Ginjal terletak di dekat bagian tengah punggung, berada tepat di bawah tulang…
- Manfaat Buah Naga untuk Kesehatan Tubuh Apa khasiat dan manfaat buah naga untuk ibu hamil dan kesehatan? Buah naga punya fisik yang cantik dan unik, dengan daging buah yang berwarna merah pekat maupun putih. Daging buahnya…
- Makromolekul : Protein Kali ini kami akan membahas materi kimia tentang asam amino pada makromolekul. Protein Merupakan polimer alam yang tersusun dari asam-asam amino melalui ikatan peptida, sehingga protein juga disebut sebagai polipeptida.…
- 16 Jenis Hormon Pada Tumbuhan Dan Fungsinya Terlengkap Penjelasan Terlengkap Tentang Jenis Jenis Hormon Pada Tumbuhan dan Fungsinya Setiap tumbuhan pasti memiliki prangsang untuk membantu pertumbuhan serta meningkatkan efisiensi dan efektivitas dalam pertumbuhan. Perangsang dalam tumbuhan disebut dengan…


