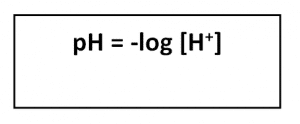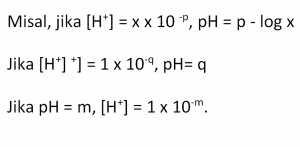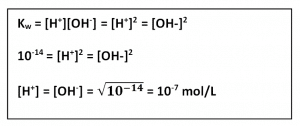Kekuatan asam atau basa suatu larutan dapat ditentukan dari harga pH, pOH, dan pKw larutannya.
Istilah pH digunakan untuk menyatakan keasaman atau kebasaan suatu larutan. Istilah pH berasal dari potential of hydrogen yang dikemukakan oleh Soren Peter Lauritz Sorensen, kimiawan dari Denmark, pada tahun 1909 yang berarti pangkat atau eksponen. Dengan demikian, pH dapat dibaca pangkat hidrogen atau eksponen hidrogen. Besarnya nilai pH adalah negatif logaritma konsentrasi ion H+.
Secara matematis, pH dinyatakan sebagai ukuran konsentrasi ion hidrogen atau [H+] dalam larutan yang dirumuskan dengan:
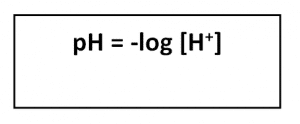
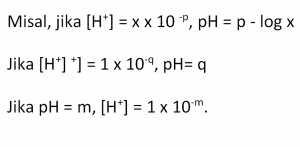
Konsentrasi ion H+ dan pH dirumuskan dengan tanda negatif. Dengan demikian, keduanya berbanding terbalik, semakin kecil konsentrasi ion H+, nilai pH semakin besar. Oleh karena bilangan dasar logaritma adalah 10 maka larutan yang nilai pH-nya berbeda sebesar x akan mempunyai perbedaan konsentrasi ion H+ sebesar 10X. Misal sebagai berikut.
Jika konsentrasi ion H+ = 0,01 M, nilai pH = -log 1 x 10-2 = 2.
Jika konsentrasi ion H+ = 0,001 M, nilai pH = -log 1 x 10-3 = 3.
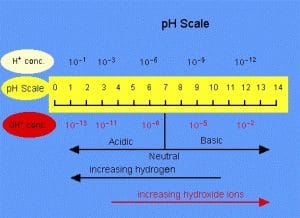
Dengan demikian, semakin besar konsentrasi ion H+ maka nilai pH semakin kecil. Larutan dengan pH = 2 keasamannya 10 kali lebih asam daripada larutan dengan pH = 3.
Penentuan pH tersebut juga berlaku untuk penentuan pOH. Konsentrasi ion OH– dinyatakan dengan pOH sehingga pOH = – log [OH–]. Misal sebagai berikut.
Jika [OH–] = 0,1 M, nilai pOH = -log 1 x 10-1 = 1.
Jika [OH–] = 0,01 M, nilai pOH = -log 1 x 10-2 = 2.
Jika pOH = 3, [OH–] = 10-3 M atau 0,001 M.
Nilai pH air murni = 7 dan disebut netral. Nilai tersebut diperoleh dari ionisasi sebagian dalam air murni. H2O(ℓ)↔ H+(aq) + OH– (aq)
Harga konstanta kesetimbangan K untuk reaksi kesetimbangan ionisasi air:
Harga [H20] dianggap tidak berubah karena air murni merupakan elektrolit yang sangat lemah. Oleh sebab itu, air murni yang terionisasi sangat kecil. Dengan demikian, K . [H2O] menjadi tetapan kesetimbangan ion bagi air yang dinotasikan dengan Kw.
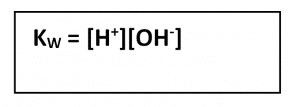
Berdasarkan hasil eksperimen, nilai pada suhu 25°C, Kw = 1 x 10-14.
Oleh karena pada ionisasi harga [H+] = [OH–], maka
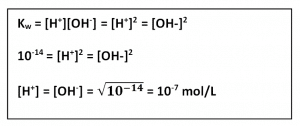
Jika persamaan di atas diubah menjadi persamaan logaritma akan diperoleh:
log Kw = log [H+] + log [OH–]
Jika persamaan ini dikalikan dengan faktor-1, menjadi:
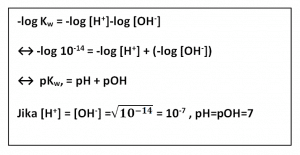
Penambahan senyawa ion H+ terlarut dari suatu asam ke dalam air akan mendesak kesetimbangan ionisasi air ke arah kiri (ion OH- akan diikat oleh H+ membentuk air). Akibatnya, terjadi kelebihan ion hidrogen sehingga konsentrasi ion H+ meningkat. Oleh sebab itu, nilai pH air < 7 atau air berubah sifat menjadi asam.
Dengan cara yang sama, penambahan senyawa ion OH- terlarut dari basa ke dalam air akan mendesak kesetimbangan air ke arah kiri. Akibatnya, ion hidroksida berlebih sehingga konsentrasi ion OH-juga meningkat. Dengan demikian, nilai pH air > 7 atau air berubah sifat menjadi basa.
Demikian penjelasan yang bisa kami sampaikan tentang Konsep pH, pOH, dan pKw Pada Larutan Asam Basa. Semoga postingan ini bermanfaat bagi pembaca dan bisa dijadikan sumber literatur untuk mengerjakan tugas. Sampai jumpa pada postingan selanjutnya.
Artikel Paling Populer :
- Hidrolisis Garam : Pengertian, Macam, Dan Rumus,… Karena pada kesempatan kali ini disini akan mengulas tentang pengertian Hidrolisis Garam, macam Hidrolisis Garam, dan rumus Hidrolisis Garam beserta contoh soalnya secara lengkap. Oleh karena itu marilah simak ulasan…
- Asam Basa – Penentuan pH Asam Kuat Dan Basa Kuat… Setelah kita mempelajari tentang pH, pOH, dan pKw, dikatakan bahwa Istilah pH digunakan untuk menyatakan keasaman atau kebasaan suatu larutan. Istilah pH berasal dari potential of hydrogen yang dikemukakan oleh…
- Pengertian dan Cara Menghitung Kemolaran, Kemolalan… Pengertian dan Cara Menghitung Kemolaran, Kemolalan dan Kenormalan Larutan Lengkap – Molaritas adalah jumlah mol zat terlarut dalam 1 liter larutan atau 1 mmol zat terlarut dalam 1 ml larutan. Satuan…
- Pengertian, Rumus dan Contoh Soal Molaritas,… Pengertian, Rumus dan Contoh Soal Molaritas, Pembuatan Larutan dan Pengenceran Lengkap – Kali ini kita aka membahas tentang pengertian dan rumus molaritas, pembuatan larutan dan pengenceran beserta dengan contoh soal dan…
- Pengertian, Ciri-Ciri dan Contoh Larutan Elektrolit… Pengertian, Ciri-Ciri dan Contoh Larutan Elektrolit dan Non Elektrolit Terlengkap – Larutan Elektrolit adalah suatu zat yang larut atau terurai dalam bentuk ion-ion dan selanjutnya larutan tersebut menjadi konduktor elektrik atau dapat menhantarkan…
- Pengertian Pangkat Tiga dan Akar Pangkat Tiga Pada postingan sebelumnya yang berjudul “Pengertian Perpangkatan Bilangan” sudah dijelaskan bahwa operasi perpangkatan merupakan perkalian berulang dengan unsur yang sama. Hal ini juga berlaku pada bilangan berpangkat tiga. Jadi, m3 =…
- Pengertian Kelarutan (k) Dan Hasil Kali Kelarutan (Ksp) Kemampuan garam larut dalam air berbeda-beda. Natrium klorida (NaCI) termasuk salah satu contoh garam yang mudah larut dalam air. Apabila NaCI dilarutkan dalam air, mula-mula akan larut. Namun, jika semakin…
- Titik Didih Mendidih merupakan peristiwa yang tepat terjadi pada suatu zat ketika berubah wujud dari cair menjadi gas. Pernahkah kamu memanaskan air di dalam panci? Maka pada suhu tertentu akan timbul gelembung-gelembung…
- Kesetimbangan Kimia Ada yang sudah mengenal atau pernah mendengar mengenai Kesetimbangan Kimia? Simak penjelasan terlengkapnnya di bawah ini. Pengertian Kesetimbangan Kimia Kesetimbangan Kimia merupakan salah satu bentuk reaksi bolak-balik yang mana laju…
- Reaksi Kesetimbangan Kimia Dalam Industri Dan… Berdasarkan azas Le Chatelier pada artikel sebelumnya, diketahui bahwa sistem yang berada dalam kesetimbangan akan selalu berusaha untuk mempertahankan kesetimbangannya. Dengan demikian, apabila terjadi aksi maka sistem akan mengalami pergeseran agar kesetimbangan tercapai…
- Unsur, Senyawa dan Campuran Setiap hari kita sering menjumpai benda-benda yang mempunyai suatu bentuk, sifat, dan struktur penyusunnya yang beda-beda. Benda-benda tersebut ada yang dibentuk dari gabungan beberapa benda dan ada pula yang tidak…
- Makalah Teori Indikator Asam Basa : Indikator, Ciri,… Air murni tidak mempunyai rasa, baud an warna. Bila mengandung zat tertentu, air dapat terasa asam, pahit, asin dan sebagainya. Air yang mengandung zat lain dapat pula menjadi berwarna. Kita…
- Faktor Faktor yang Mempengaruhi Pergeseran… Henry Louis Le Chatelier (1850-1936), ilmuwan kimia dari Prancis, pada tahun 1884 menyatakan bahwa ’’apabila dalam suatu kesetimbangan dilakukan tindakan (aksi) maka sistem kesetimbangan tersebut akan mengadakan reaksi sehingga pengaruh…
- Asam Basa – Peranan dan Pemanfaatan Asam Basa dalam… Asam-basa sangat berkaitan erat dengan kehidupan sehari-hari. Sifat asam-basa tidak hanya berperan dalam bidang kimia, tetapi juga sangat berguna dalam berbagai bidang keilmuan seperti kedokteran, biologi, dan arkeologi. Pemanfaatan Sifat…
- Sistem Koloid – 8 Sifat Koloid Dan Penjelasan Terlengkap Koloid merupakan campuran yang berada di antara campuran homogen dan heterogen. Oleh karena itu, koloid mempunyai sifat-sifat khusus yang tidak dimiliki oleh campuran homogen dan campuran heterogen. Penjelasan beberapa sifat…
- Sifat Koligatif Larutan Sifat larutan yang mengakibatkan berubahnya berubahnya tekanan osmotik, titik beku, titik didih, dan lainnya Pendahuluan Saat kalian mencapur pelarut dan terlarut, kalian akan mendapatkan larutan. WOW keren banget ya! Nggak…
- Contoh Zat Kimia Sebagai Pengawet Makanan dan Minuman Bahan pengawet adalah bahan kimia yang dapat mencegah atau menghambat proses fermentasi (pembusukan), pengasaman, atau peruraian lain terhadap makanan yang disebabkan oleh mikroorganisme sehingga makanan tidak mudah rusak atau menjadi busuk.…
- Makromolekul : Asam Amino Kali ini kami akan membahas materi kimia tentang asam amino pada makromolekul. Asam Amino Asam amino ialah senyawa yang mempunyai gugus asam karbosilat (-COOH) dan gugus amina (-NH2). Rumus umum…
- Sistem Dispersi Ada yang sudah mengenal atau pernah mendengar mengenai istilah Sistem Dispersi? Simak penjelasan terlengkapnnya di bawah ini. Pengertian Sistem Dispersi Sistem dispersi merupakan salah satu campuran antara zatterlarut dan pelarut.…
- Prinsip Kerja Larutan Penyangga Dan Sifat – Sifat… Lensa kontak sering digunakan sebagai pengganti kacamata atau sekadar untuk mempercantik penampilan. Lensa kontak tidak dapat digunakan secara sembarangan. Lensa kontak mempunyai pH tertentu yang tidak boleh berubah. pH lensa…