Telah kita pelajari tentang pengertan termokimia pada postingan sebelumnya. Bahwa Termokimia adalah cabang ilmu kimia yang mempelajari tentang perubahan kalor atau energi yang menyertai suatu reaksi kimia, baik yang diserap maupun yang dilepaskan. Untuk lebih lengkap nya.

Dibawah ini admin sajikan beberapa contoh soal dan pembahasannya tentang materi termokimia.
Soal No.1
Diketahui 1 mol NO terurai menjadi unsur-unsur pembentuknya dengan melepaskan kalor sebesar 90,4 kJ.
a. Tuliskan persamaan termokimia dari reaksi tersebut!
b. Gambarkan diagram tingkat energinya!
c. Tentukan perubahan entalpi untuk reaksi pembentukan 1,5 mol zat tersebut dan persamaan termokimianya!
Pembahasan:
a. Reaksi penguraian NO melepaskan kalor. Dengan demikian, perubahan entalpinya berharga negatif. Persamaan termokimia untuk 1 mol NO sebagai berikut.
NO(g) → ⅟2 N2(g) + ⅟2 O2(g) ∆H = -90,4 kJ/mol
b. Diagram tingkat energinya:
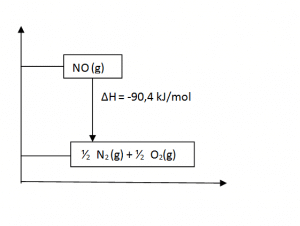
c. Perubahan entalpi pembentukan untuk 1,5 mol NO sebagai berikut.
Reaksi pengurai:
NO(g) → ⅟2 N2(g) + ⅟2 O2(g) ∆H = -90,4 kJ/mol
Reaksi pembentukan:
NO(g) → ⅟2 N2(g) + ⅟2 O2(g) ∆H = -90,4 kJ/mol
untuk 1,5 mol NO perubahan entalpinya sebesar 1,5 x 90,4 kJ = 135,6 kJ.
Jadi, persamaan termokimia untuk pem-bentukan 1,5 mol NO sebagai berikut.
N2(g) + O2(g) → 2NO(g) ∆H = + 135,6 kJ
Soal No.2
Kelompokkan reaksi-reaksi di bawah ini ke dalam reaksi endoterm atau reaksi eksoterm!
a. N204 (g) → 2N02(g) ∆H = +58 kJ
b. N2(g) + 3H2(g) → 2NH3(g) ∆H = -92 kJ
c. HCI(aq) + NaOH(aq) → NaCI(aq) + H20(ℓ) ∆H = -56 kJ
d. 2C(s) + H2(g) → C2H2(g) ∆H = +225 kJ
Pembahasan:
Reaksi:
- 2C(s) + H2(g) → C2H2(g) ∆H = +225kJ
- N204(g) → 2NO2(g) ∆H = +58 kJ
Termasuk reaksi endoterm karena memiliki ∆H positif. Sementara itu, reaksi:
- HCI(aq) + NaOH(aq) → NaCI(aq) + H20(ℓ) ∆H = -56 kJ
- N2(g) + 3H2(g) → 2NH3(g) ∆H = -92kJ
Termasuk reaksi eksoterm karena memiliki AH negatif.
Soal No.3
Diketahui entalpi pembentukan 14 g gas etilena (C2H4) adalah +26,15kJ.
a. Berapakah besarnya kalor yang dilepaskan untuk menguraikan 84 g gas etilena menjadi unsur-unsurnya?
b. Tuliskan persamaan termokimianya!
Pembahasan:
Perbandingan koefisien = perbandingan mol

Soal No.4
Diketahui persamaan termokimia reaksi pembakar- an gas asetilen (C2H2) sebagai berikut.
2C2H2(g) + 502(g) → 4C02(g) + 2H20(ℓ)
∆H = -2.599,1 kJ.
a. Tentukan entalpi pembakaran standar gas asetilen!
b. Hitung kalor yang dihasilkan pada pembakaran 10 L gas asetilen!
Pembahasan:
a. Entalpi pembakaran standar gas asetilen sebagai berikut.
Reaksi pembakaran pada persamaan reaksi 2C2H2 + 5O2 -+ 4CO2+ 2H2O menunjukkan bahwa pembakaran tersebut dilakukan untuk 2 mol gas C2H2, dengan membebaskan kalor sebesar 2.599,1 kJ. Oleh karena itu, entalpi pembakaran standar gas asetilen harus ditentukan untuk 1 mol gas asetilen. Dengan demikian, besarnya entalpi pembakaran standar gas asetilen adalah 2.599,1 kJ : 2 = 1.299,6 kJ.
b.Besarnya kalor yang dihasilkan pada pem-bakaran 10 L gas asetilen sebagai berikut. mol gas asetilen pada kondisi standar:

Soal No.5
Diketahui entalpi pembentukan standar (∆H°f) H20(ℓ) = -285,85 kJ/mol. Berapakah kalor yang diperlukan untuk menguraikan 13 gram air menjadi hidrogen dan oksigen pada keadaan standar? (Ar H = 1, Ar O = 16)
Pembahasan:
AH°f H20(ℓ) = -285,85 kJ/mol
Persamaan termokimia reaksi pembentukan H20:
H2(g) + ⅟2 O2(g) →H20(ℓ) ∆H = -285,85 kJ/mol.
Persamaan termokimia reaksi penguraian H20(ℓ)
H20(ℓ) →H2(g) + ⅟2 O2(g) ∆H =+285,85 kJ/mol.
Jumlah mol air dalam 10 gram air = 13 g /18g/mol – 0,72 mol.
Kalor yang diperlukan untuk menguraikan 13 g air = 0,72 mol/ 1 mol x 285,85 kJ/mol = 205,812 kJ/mol
Jadi, kalor yang diperlukan untuk menguraikan 13 gram air menjadi hidrogen dan oksigen sebesar 205,812 kJ.
Artikel Paling Populer :
- Pengertian , Struktur, Sistem Kerja dan Faktor yang… Pengertian , Struktur, Sistem Kerja dan Faktor yang Memengaruhi Kerja Enzim Pada Sistem Metabolisme Metabolisme adalah semua reaksi kimia yang terjadi pada sel hidup, Metabolisme meliputi Katabolisme dan Anabolisme. Katabolisme adalah…
- Jenis-Jenis Energi Ada yang sudah mengenal atau pernah mendengar mengenai istilah Energi? Simak penjelasan terlengkapnnya di bawah ini. Pengertian Energi Energi berasal dari bahasa Yunani yakni “ergon” yang artinya kerja. Dalam melakukan…
- Pengertian Kuadrat dan Akar Kuadrat Bilangan Bulat Pada saat ditingkat SD/MI Anda telah mempelajari kuadrat dan akar kuadrat bilangan bulat. Sekarang pada postingan ini kembali mengulas tentang materi kuadrat dan akar kuadrat dengan tujuan untuk mengingatkan kepada…
- Rumus Dan Pembahasan Contoh Soal Persamaan Lingkaran… Rumus Dan Pembahasan Contoh Soal Persamaan Lingkaran Matematika Lingkaran adalah tempat kedudukan atau himpunan titik titik yang berjarak sama terhadap suatu titik tertentu. Titik tertentu tersebut dinamakan pusat lingkaran dan…
- Pengertian Energi, Daya Listrik Dan Daya Elemen… Dalam kehidupan modern, listrik merupakan salah satu kebutuhan manusia. Banyak peralatan listrik yang kita gunakan dalam kehidupan sehari-hari. Di daerah yang belum terjangkau instalasi listrik pun telah memanfaatkan listrik. Misalnya,…
- Berbagai Cara Penentuan Perubahan Entalpi Reaksi Dan… Perubahan entalpi reaksi (ΔH) dapat ditentukan dengan berbagai cara, yaitu menggunakan kalorimeter, data entalpi pembentukan standar, diagram tingkat energi (hukum Hess), dan energi ikatan.Dibawah ini akan kita jelaskan secara rinci…
- Perubahan Kimia Perubahan kimia yang berhubungan dengan mudah sukarnya benda bereaksi kimia. Dalam kehidupan sehari-hari misalnya nasi yang menjadi basi karena terjadi adanya perubahan kimia. Untuk lebih jelas lagi mari simak ulasan…
- 8 Macam Perubahan Entalpi Dan Penjelasan Terlengkap Postingan sebelumnya admin telah membahas tuntas tentang Termokimia – Pengertian, Reaksi Termokimia dan Perubahan Entalpi. Kali ini akan membahas macam-macam perubahan entalpi secara lengkap dengan penjelasannya. Perubahan entalpi yang menyertai suatu reaksi…
- Pengertian, Rumus, Kapasitas dan Perpindahan Kalor… Pengertian, Rumus, Kapasitas dan Perpindahan Kalor Dan Kalor Jenis Terlengkap – Kalor yaitu salah satu bentuk energi yang bisa berpindah dari satu benda ke benda yang lainnya karena adanya suatu…
- Faktor Faktor yang Mempengaruhi Pergeseran… Henry Louis Le Chatelier (1850-1936), ilmuwan kimia dari Prancis, pada tahun 1884 menyatakan bahwa ’’apabila dalam suatu kesetimbangan dilakukan tindakan (aksi) maka sistem kesetimbangan tersebut akan mengadakan reaksi sehingga pengaruh…
- Contoh Soal Kimia Dan Pembahasan Terlengkap Tentang… Setelah kita mempelajari tentang materi reaksi kesetimbangan pada postingan artikel sebelumnya, kali ini pembahasan selanjutnya mengenai soal tentang reaksi kesetimbangan. 1. Golongkan reaksi-reaksi berikut ke dalam reaksi homogen atau heterogen!…
- Makromolekul : Protein Kali ini kami akan membahas materi kimia tentang asam amino pada makromolekul. Protein Merupakan polimer alam yang tersusun dari asam-asam amino melalui ikatan peptida, sehingga protein juga disebut sebagai polipeptida.…
- Pengertian Teori Tumbukan dan Faktor-Faktor yang… Reaksi kimia terjadi ketika partikel-partikel zat yang bereaksi (pereaksi) saling bertumbukan. Namun, tidak semua tumbukan yang terjadi akan menghasilkan zat baru. Zat baru dapat dihasilkan dari tumbukan yang berlangsung sempurna.…
- Menyelesaikan Masalah Dengan Menggunakan Konsep Himpunan Jika Anda amati masalah dalam kehidupan sehari-hari maka banyak di antaranya dapat diselesaikan dengan konsep himpunan. Agar dapat menyelesaikannya, Anda harus memahami kembali mengenai konsep diagram Venn dan Anda harus dapat menyatakan permasalahan…
- Mempelajari Sejarah Perkembangan Ilmu Kimia Terlengkap Sekitar tahun 3500 SM, peradaban Mesir kuno sudah mempraktikan reaksi kimia. Pada masa itu telah diketahui cara membuat anggur, pengawetan mayat, dan pengolahan beberapa logam seperti tembaga dan timah Sekitar…
- Penyelesaian Persamaan Linear Satu Variabel Bentuk Pecahan Dalam menyelesaikan persamaan linear satu variabel (PLSV) yang berbentuk pecahan caranya hampir sama seperti mengerjakan PLSV yang bentuknya bukan pecahan yang sudah dibahas pada postingan sebelumnya dan tetnunya cara tersebut hampir sama…
- Pengertian, Rumus dan Contoh Soal Molalitas dan… Pengertian, Rumus dan Contoh Soal Molalitas dan Fraksi Mol Lengkap – Molalitas atau kosentrasi molal adalah ukuran konsentrasi dari suatu zat terlarut di dalam suatu larutan dalam hal jumlah zat dalam…
- Reaksi Anabolisme – Penjelasan Lengkap Tahap dan… Reaksi Anabolisme – Penjelasan Lengkap Tahap dan Faktor-Faktor Fotosintesis dan Kemosintesis Telah kita pelajari pada postingan sebelumnya mengenai metabolisme, enzim dan katabolisme pada postingan sebelumnya. Kali ini kita akan membahas…
- Mempelajari Sistem Persamaan Linier Dan Metode… Sistem persamaan linier sebenarnya hampir sama dengan persamaan aljabar, yakni sebuah sistem penghitungan yang menggunakan metode matematika dan juga dapat di gambarkan dengan menggunakan bentuk garis lurus dalam sebuah grafik.…
- Unsur Oksigen Hai sobat hitung, bagaimana kabarnya? Semoga tetap sehat dan semangat ya… Nah, kali ini kami akan menjelaskan sedikit tentang materi kimia, yaitu mengenai unsur oksigen dan nitrogen. Harus kalian ketahui…



