Pengertian, Rumus dan Contoh Soal Molaritas, Pembuatan Larutan dan Pengenceran Lengkap – Kali ini kita aka membahas tentang pengertian dan rumus molaritas, pembuatan larutan dan pengenceran beserta dengan contoh soal dan penyelesaiannya. Berikut penjelasan selengkapnya:
A. Molaritas
Konsentrasi ialah jumlah zat terlarut yang hadir terhadap jumlah pelarut tertentu atau terhadap jumlah larutan tertentu. (Dalam hal ini kita dapat mengasumsikan zat terlarut berwujud cair atau padat, sedangkan pelarutnya berwujud zat cair) Konsentrasi bisa diungkapkan dengan berbagai cara, salah satunya yang paling sering dipakai, dan memang akan kita gunakan sekarang ini yaitu Molaritas (M), atau konsentrasi molar. Molaritas ialah jumlah mol terlarut setiap liter larutan. Atau bisa diungkapkan dengan menggunakan rumus:
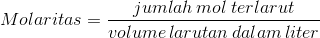
Atau bisa juga diungkapkan sebagai:
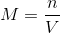
Dimana n menunjukan tentang jumlah mol zat terlarut (ingat ya zat terlarut) dan V menunjukan tentang volume larutan dalam liter (jangan lupa larutan dalam liter). Nah apabila yang diketahuinya bukan mol tapi melainkan gram zat terlarut, rumus tadi dapat juga diungkapkan dengan:
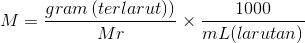
Satu lagi, apabila yang diketahui adalah massa jenis larutan (ρ) dan kadar atau persen massa (%), maka Molaritas bisa dicari dengan menggunakan rumus seperti:
Contoh:
1,46 molar larutan Glukosa (C6H12O6), ditulis dengan 1,46 M C6H12O6, yang artinya adalah mengandung 1,46 mol zat terlarut (C6H12O6) di dalam1 liter larutan (pelarut+terlarut). Tentu saja dalam hal ini volumenya tidak harus 1 liter, yang penting perbandingannya sama. Misalnya apabila volume larutan 500 mL (0,5L), maka C6H12O6 yang terlarut yaitu sebanyak 0,73 mol.
B. Pembuatan larutan
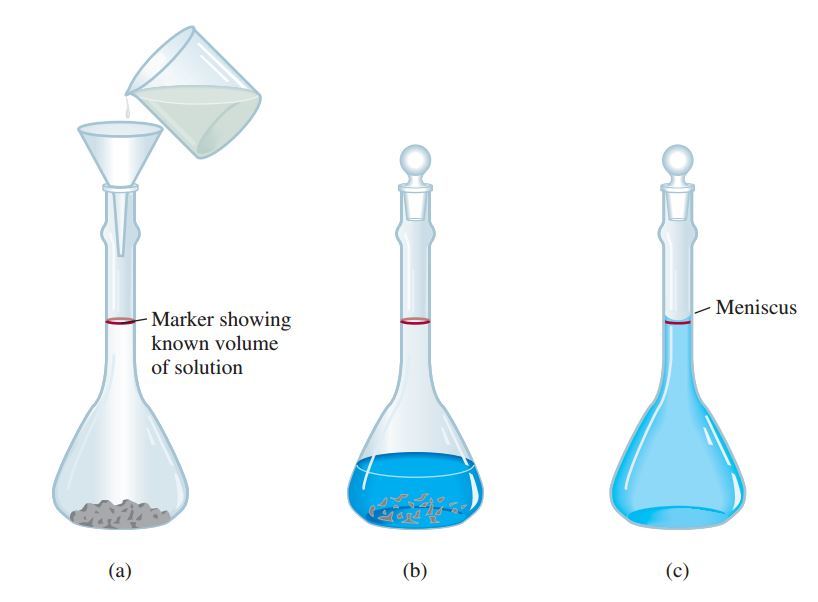
“masukan terlebih dahulu padatan, kemudian isi sedikit air. setelah larut baru tambahkan lagi air sampai batas garis”
Untuk membuat suatu larutan, yang tentunya nanti berhubungan langsung dengan molaritas. Langkah pertama yaitu memasukan zat terlarut yang sudah ditimbang terlebih dahulu (biasanya dalam bentuk padatan dengan massa dalam ukuran gram) ke dalam labu ukur melalui sebuah corong. Langkah selanjutnya adalah menambahkan sedikit air ke dalam labu ukur dengan perlahan hingga zat terlarut melarut sambil digoyang-goyangkan. Setelah zat terlarut tersebut sepenuhnya melarut, selanjutnya yaitu tambahkan sedikit demi sedikit air, dan jangan sampai melewati garis batas yang ada di labu ukur.
Dengan mengetahui suatu volume larutan yang dimasukkan ke dalam labu ukur, dan juga mengetahui jumlah dari zat terlarut (biasanya diukur dalam gram, sehingga nantinya biasa dirubah ke satu mol dengan rumus mol=gram/Mr) maka kita akan bisa menghitung Molaritas larutan tersebut.
C. Pengenceran
Seringkali larutan dibuat dan disimpan di dalam laboratorium dengan konsentrasi yang tinggi sebagai larutan ‘stok’. Hal ini akan lebih menghemat waktu daripada harus selalu membuat larutan setiap praktikum. Larutan ‘stok’ ini nantinya tinggal diambil sedikit, yang kemudian diencerkan sehingga konsentrasinya menjadi lebih kecil sesuai dengan kebutuhan. Oleh karena itu kita harus mengetahui cara mengencerkan larutan tersebut.
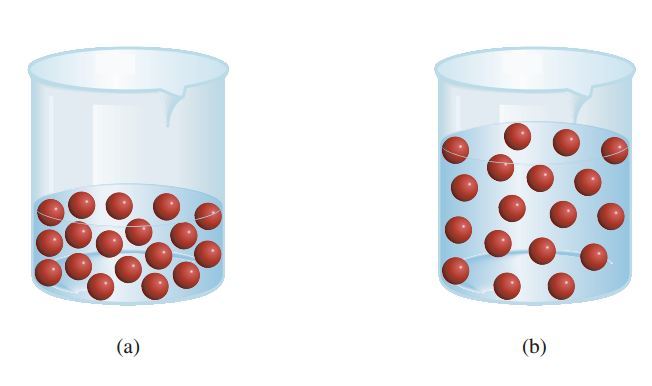
“(a) sebelum diencerkan, (b) seseudah diencerkan”
Ketika dilakukan sebuah pengenceran, sebenarnya jumlah mol zat terlarut tidaklah berubah, melainkan yang mengalami perubahan hanyalah volumenya saja. Mari kita lihat ilustrasinya
Jika terdapat 18 molekul terlarut sebelum diencerkan, maka ketika ditambahkan air, jumlah si molekul terlarut ini tidak akan berubah bukan? Ya tetap jumlahnya akan 18 molekul. Begitu juga dengan jumlah mol, tidak akan berubah. Sehingga, akan berlaku
nsebelum pengenceran = nsesudah pengenceran
dan berdasarkan rumus molaritas sebelumnya, dimana n =M.V, maka:
n1 = n2
M1 V1 = M2 V2
Dimana M1 adalah konsentrasi awal sebelum pengenceran dan M2 adalah kkonsentrasi larutan sesudah pengenceran.
Contoh soal
Berapakah Volume dari larutan H2SO4 2 M yang dibutuhkan untuk membuat larutan 200 mL H2SO4 0,5 M?
Jawab:
M1= 2 M, V1 = …?
M2 = 0,5 M, V2 = 200 mL
Maka:
M1 V1 = M2 V2
2 . V1 = 0,5 . 200
V1 = 50 mL
Demikian pembahasan tentang”Pengertian, Rumus dan Contoh Soal Molaritas, Pembuatan Larutan dan Pengenceran Lengkap” , semoga bermanfaat.
Artikel Paling Populer :
- Penerapan Operasi Hitung Bilangan Bulat operasi hitung pada bilangan bulat yang meliputi operasi penjumlahan, operasi pengurangan, operasi perkalian dan oprasi pembagian. Semua operasi tersebut sekarang kita terapkan pada contoh soal untuk menyelesaikan masalah yang berkaitan dengan kehidupan sehari-hari. Berikut contoh…
- Laju Reaksi : Pengertian, Rumus, Contoh Soal Dan… Laju Reaksi : Pengertian, Faktor Yang Mempengaruhi, Dan Rumus Beserta Contoh Soalnya Lengkap Konsep pembelajaran kimia merupakan konsep yang erat dengan kehidupan sehari hari. Kimia menggambarkan kehidupan sedemikian rupa sehingga…
- Molaritas, Molalitas, Normalitas, Fraksi Mol Ada yang sudah mengenal atau pernah mendengar mengenai Molaritas, Molalitas, Normalitas, dan Fraksi Mol? 1. Mol Larutan (n) Mol merupakan massa (gram) pada suatu zat dibagi dengan massa molekul relatif atau berat…
- Pengertian, Rumus dan Contoh Soal Mol, Molalitas,… Pengertian, Rumus dan Contoh Soal Menghitung Mol, Molalitas, Molaritas, Normalitas, Part Per Million (ppm), Persen Massa dan Persen Volume Larutan Lengkap – Dalam kimia, ada beberapa satuan yang sering digunakan untuk…
- Contoh Soal Kimia Dan Pembahasan Terlengkap Tentang… Setelah kita mempelajari tentang materi reaksi kesetimbangan pada postingan artikel sebelumnya, kali ini pembahasan selanjutnya mengenai soal tentang reaksi kesetimbangan. 1. Golongkan reaksi-reaksi berikut ke dalam reaksi homogen atau heterogen!…
- Asam Basa – Penentuan pH Asam Kuat Dan Basa Kuat… Setelah kita mempelajari tentang pH, pOH, dan pKw, dikatakan bahwa Istilah pH digunakan untuk menyatakan keasaman atau kebasaan suatu larutan. Istilah pH berasal dari potential of hydrogen yang dikemukakan oleh…
- Kromatografi Adalah Ada yang sudah mengenal atau pernah mendengar mengenai istilah Kromatografi? Simak penjelasan terlengkapnnya di bawah ini. Pengertian Kromatografi Kromatografi merupakan suatu teknik pemisahan molekul berdasarkan perbedaan pola pergerakan antara fase…
- Apa Contoh Bahan Kimia Sebagai Pemutih Pernahkah anda mencuci baju dengan deterjen tetapi nodanya masih menempel pada baju. Apa yang anda lakukan agar noda tersebut lenyap di baju? Cara yang paling mudah menghilangkan noda baju adalah dengan menggunkan…
- Pengertian Dan Macam – Macam Larutan Penyangga Air liur merupakan pelindung alami bagi kesehatan gigi. Ketika terjadi sekresi dan kontak langsung dengan gigi, air liur akan menetralkan asam yang terbentuk dari proses fermentasi sisa makanan dimulut dan…
- Hidrolisis Garam : Pengertian, Macam, Dan Rumus,… Karena pada kesempatan kali ini disini akan mengulas tentang pengertian Hidrolisis Garam, macam Hidrolisis Garam, dan rumus Hidrolisis Garam beserta contoh soalnya secara lengkap. Oleh karena itu marilah simak ulasan…
- Pengertian Tritrasi,Stoikiometri Larutan Dan Grafik… Titrasi asam-basa merupakan suatu cara yang cukup teliti untuk menentukan konsentrasi suatu asam atau basa. Konsentrasi suatu asam ditentukan dengan cara menitrasi asam dengan basa yang telah diketahui kadarnya, begitu…
- Pengertian, Rumus dan Contoh Soal Listrik Dinamis… Pengertian, Rumus dan Contoh Soal Listrik Dinamis Beserta Cara Penyelesaian Lengkap – Listrik dinamis (electronidinamic) berasal dari perpaduan kata listrik dan dinamis. Listris adalah listrik, sedangkan dinamis yaitu berubah-ubah atau bergerak.…
- Pengertian Reaksi Kimia, Kesetimbangan Kimia, dan… Pernahkah Anda mengamati keadaan gua? Pada umumnya, keadaan di dalam gua adalah lembap, banyak tetesan air, stalaktit, dan stalakmit. Stalaktit dan stalakmit terbentuk dari endapan mineral kalsium karbonat (CaCO3). Endapan…
- Pengertian, Ciri-Ciri dan Contoh Larutan Elektrolit… Pengertian, Ciri-Ciri dan Contoh Larutan Elektrolit dan Non Elektrolit Terlengkap – Larutan Elektrolit adalah suatu zat yang larut atau terurai dalam bentuk ion-ion dan selanjutnya larutan tersebut menjadi konduktor elektrik atau dapat menhantarkan…
- Filtrasi Adalah Ada yang sudah mengenal atau pernah mendengar mengenai istilah Filtrasi? Simak penjelasan terlengkapnnya di bawah ini. Pengertian Filtrasi Filtrasi merupakan salah satu metode atau sebuah cara pemisahan secara fisik atau…
- Pengertian, Sifat, Rumus dan Contoh Soal Tekanan… Pengertian, Sifat, Rumus dan Contoh Soal Tekanan Hidrostatis Beserta Pembahasan Terlengkap – Tekanan hidrostatis adalah tekanan yang diakibatkan oleh gaya yang ada pada zat cair terhadap suatu luas bidang tekan…
- Destilasi Adalah Ada yang sudah mengenal atau pernah mendengar mengenai istilah Destilasi? Simak penjelasan terlengkapnnya di bawah ini. Pengertian Destilasi Distilasi (Penyulingan) merupakan sebuah metode yang dipakai memisahkan bahan kimia menurut perbedaan…
- Bola – Ciri, Contoh Soal Beserta Penyelesaian Luas… Bola – Ciri, Contoh Soal Beserta Penyelesaian Luas Permukaan dan Volume Bola Lengkap – Bola merupakan bangun ruang tiga dimensi yang dibentuk oleh titik-titik yang berjarak sama terhadap suatu titik yang…
- DIAGRAM FASE ZAT Dan Penerapan sifat koligatif larutan DIAGRAM FASE ZAT Membandingkan sifat koligatif antara dua larutan atau lebih Kondisi Perbandingan [Larutan elektrolit] = [larutan nonelektrolit] Tf larutan nonelektrolit > larutan elektrolit Tb larutan elektrolit > larutan nonelektrolit [Larutan elektrolit] ≠ [larutan…
- Cara Pembuatan Koloid – Cara Kondensasi Dan Cara… Sistem koloid berada di antara larutan sejati dan suspensi. Jadi, susu merupakan koloid yang berada di antara larutan gula (larutan sejati) dan campuran air dengan pasir (suspensi). Oleh karena itu,…
![]()
![]()
![]()

