Setiap molekul yang tersusun dari atom unsur tertentu dengan jumlah yang tertentu pula akan mempunyai bentuk molekul tertentu. Bentuk molekul merupakan bentuk geometris yang terjadi jika inti atom unsur yang saling berikatan dalam suatu molekul dihubungkan dengan suatu garis lurus. Bentuk molekul senyawa kovalen ditentukan oleh susunan ruang pasangan elektron di sekitar atom pusat.
Bentuk molekul senyawa kovalen diuraikan berdasarkan dua teori yaitu teori domain elektron (VSEPR) dan teori hibridisasi.
Teori Domain Elektron
Domain elektron adalah suatu area dalam molekul yang ditempati oleh elektron. Teori domain elektron menyatakan bahwa pasangan elektron ikatan dan pasangan elektron bebas tolak-menolak sehingga tiap-tiap pasangan elektron cenderung berjauhan satu sama lain untuk meminimalkan gaya tolakan tersebut. Jadi, bentuk molekul dipengaruhi oleh susunan ruang pasangan elektron ikatan (PEI) dan pasangan elektron bebas (PEB) pada atom pusat suatu molekul. Teori ini juga dikenal dengan teori VSEPR (Valence Shell Electron Pair Repulsion) atau teori Tolakan Pasangan Elektron Valensi. Teori VSEPR pertama kali dikembangkan oleh ahli kimia Kanada, R.J. Gillespie pada tahun 1957 berdasarkan ide ahli kimia Inggris, N. Sigewick dan H. Powel.
Teori domain elektron merupakan penyempurnaan dari teori VSEPR. Domain elektron berarti kedudukan elektron atau daerah keberadaan elektron dengan jumlah domain sebagai berikut.
a. Setiap elektron ikatan, baik ikatan tunggal, rangkap dua, atau rangkap tiga. merupakan 1 domain.
b. Setiap pasangan elektron bebas merupakan 1 domain.
Bentuk molekul hanya ditentukan oleh pasangan elektron terikat. Terdapat lima macam bentuk dasar molekul kovalen sebagai berikut.
- Linear: bentuk molekul yang disusun oleh tiga atom yang berikatan dalam satu garis lurus dan sebuah atom merupakan pusatnya. Sudut ikat pada dua pasang elektron ikatan sebesar 180°. Contoh senyawa linear di antaranya HgBr2, CdCI2, dan BeH2
- Segitiga datar: bentuk molekul segitiga sama sisi yang disusun oleh empat buah atom. Sebuah atom sebagai pusatnya berikatan dengan tiga atom lainnya dengan sudut ikat 120°. Contoh senyawa segitiga datar yaitu BCI3, BF3, dan Gal3
- Tetrahedral: bentuk molekul yang tersusun dari lima atom berikatan. Sebuah atom sebagai pusat yang berikatan dengan empat atom lainnya dengan sudut ikat 109,5°. Contoh senyawa tetrahedral yaitu CCI4, CH4, dan SnCI4
- Trigonal bipiramida: bentuk molekul terdiri atas dua bentuk piramida yang bergabung dalam salah satu bidang. Atom pusatnya dikelilingi oleh lima atom lain dengan sudut ikat ekuatorial 120°, dan sudut aksial 90°. Contoh senyawa trigonal bipiramida yaitu PF5, SbCI5, dan PCI5
- Oktahedral: bentuk molekul terdiri atas delapan bidang yang merupakan segitiga sama sisi dengan sudut ikat 90°. Contoh senyawa oktahedral adalah SF6, TeF6, dan SeF6
Bentuk Molekul Teori Domain Elektron
Metode yang dapat digunakan untuk meramalkan bentuk molekul adalah model rumus titik elektron yang diperluas menjadi teori domain elektron atau teori tolakan pasangan elektron kulit valensi (VSEPR, Valence Shell Electron Pair Repulsion). Seperangkat aturan dikemas ke dalam teori domain elektron yang memungkinkan Anda dapat meramalkan bentuk molekul secaratepat. Teori ini didasarkan pada jumlah pasangan elektron ikatan dan pasangan elektron bebas dalam kulit valensi atom pusat suatu molekul. Teori ini menyatakan bahwa bentuk molekul dapat ditentukan berdasarkan tolakan pasangan elektron dalam kulit valensi atom pusat. Oleh karena itu, teori ini disebut domain elektron atau VSEPR. Bagaimana teori ini dapat diterapkan untuk memprediksi bentuk suatu molekul? Untuk mempermudah mempelajarinya, molekul-molekul dikelompokkan ke dalam tiga kategori, yaitu molekul-molekul yang memiliki atom pusat:
1. berikatan kovalen tunggal yang jenuh;
2. berikatan kovalen tunggal yang tidak jenuh (memiliki elektron bebas);
3. berikatan kovalen rangkap.
Dalam teori VSEPR, gaya tolakan yang dihasilkan PEB juga mempengaruhi bentuk mlekul. Notasi VSEPR yang menunjukan jumlah PEI dan PEb sebagai berikut:

Hubungan antara PEI dan PEB pada atom pusat terhadap bentu molekul disajikan dalam tabel berikut ini.

Teori Hibridilasi
Teori hibridilasi dijelaskan berdasarkan proses penggabungan orbital-orbital atom yang digunakan oleh elektron-elektron yang saling berikata. Teori ini disebut juga teori ikatan valensi.
a. Orbital Hibrida sp
b. orbital sp2
c. orbital sp3
d. orbital sp3d dan sp3d2
Secara ringkas berbagai tipe hibridasi digambarkan seperti tabel dibawah ini.
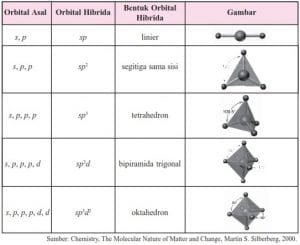
Demikian penjelasan yang bisa kami sampaikan tentang Berbagai Bentuk Molekul, Pengertian Teori Domain Elektron Dan Teori Hibridisasi. Semoga postingan ini bermanfaat bagi pembaca dan bisa dijadikan sumber literatur untuk mengerjakan tugas. Sampai jumpa pada postingan selanjutnya.
Artikel Paling Populer :
- Pengertian Asam Basa, Sifat, Teori dan Contoh Reaksi… Pengertian Asam Basa, Sifat, Teori dan Contoh Reaksi Asam Basa Terlengkap – Tentu saja kita sering mendengar istilah asam basa dalam kimia. Kata asam berasal dari bahasa Latin acidu” yang berarti…
- Pengertian Teori Tumbukan dan Faktor-Faktor yang… Reaksi kimia terjadi ketika partikel-partikel zat yang bereaksi (pereaksi) saling bertumbukan. Namun, tidak semua tumbukan yang terjadi akan menghasilkan zat baru. Zat baru dapat dihasilkan dari tumbukan yang berlangsung sempurna.…
- Laju Reaksi Ada yang sudah mengenal atau pernah mendengar mengenai Laju Reaksi? Oke, mari simak penjelasan secara lengkapnya dibawah ini ya. Pengertian Laju Reaksi Laju Reaksi ialah sebuah laju penurunan ( reaktan atau…
- Perkembangan Teori Atom Menurut Ahli : Teori… Istilah atom muncul sejak sebelum masehi yang pertama kali dikenalkan oleh Demokritus. Setiap zat terdiri dari bagian-bagian yang sangat kecil yang tidak dapat dibagi-bagi lagi, bagian yang sudah tidak dapat…
- Pengertian Teori Tumbukan dan Faktor-Faktor yang… Reaksi kimia terjadi ketika partikel-partikel zat yang bereaksi (pereaksi) saling bertumbukan. Namun, tidak semua tumbukan yang terjadi akan menghasilkan zat baru. Zat baru dapat dihasilkan dari tumbukan yang berlangsung sempurna.…
- Pengertian DNA dan RNA, Fungsi, Struktur dan… Pengertian DNA dan RNA, Fungsi, Struktur dan Jenisnya Terlengkap – Kali ini kita akan membahas tentang DNA (Deoxyribonucleic acid) dan RNA (Ribonucleic acid), serta fungsi, struktur atau komponen penyusun dan jenisnya lengkap.…
- Unsur Oksigen Hai sobat hitung, bagaimana kabarnya? Semoga tetap sehat dan semangat ya… Nah, kali ini kami akan menjelaskan sedikit tentang materi kimia, yaitu mengenai unsur oksigen dan nitrogen. Harus kalian ketahui…
- Atom Berelektron Banyak – Bilangan Kuantum Utama,… Setelah kita bahas tentang perkembangan teori atom, disebutkan bahwa teori atom mengalami perkembangan yang pesat, dari hasil percobaan menunjukkan bahwa atom masih terdiri dari partikel – partikel yang lebih kecil…
- Pengertian Senyawa, Macam-Macam, Aturan Penulisan… Pengertian Senyawa, Macam-Macam, Aturan Penulisan dan Contoh Senyawa Lengkap – Ketika sedang memasak, kita memakai air, garam, gula, maupun penyedap rasa lainnya. Zat-zat tersebut merupakan contoh dari senyawa. Air tersusun oleh…
- Tabel Periodik Unsur Kimia : Pengertian, Gambar dan… Gambar Tabel Periodik Unsur Kimia – Unsur kimia adalah zat kimia yang tidak dapat diubah lagi menjadi zat yang kecil atau dapat juga diartikan zat yang tidak dapat dibagi lagi jika…
- Berbagai Cara Penentuan Perubahan Entalpi Reaksi Dan… Perubahan entalpi reaksi (ΔH) dapat ditentukan dengan berbagai cara, yaitu menggunakan kalorimeter, data entalpi pembentukan standar, diagram tingkat energi (hukum Hess), dan energi ikatan.Dibawah ini akan kita jelaskan secara rinci…
- Ikatan Kovalen ahukah anda apa yang dimaksud dengan ikatan kovalen ??? Jika anda belum mengetahuinya anda tepat sekali mengunjungi gurupendidikan.com. Karena pada kesempatan kali ini akan membahas tentang pengertian ikatan kovalen, jenis-jenis…
- Unsur Nitrogen Definisi Nitrogen Nitrogen merupakan unsur kimia dalam tabel periodik yang mempunyai lambang N dan nomor atom 7. Unsur ini biasanya ditemukan dalam bentuk gas tanpa warna dan bau. Merupakan gas…
- Karbon Monoksida: Pengertian, Struktur, Reaksi,… Dalam rumus kimia CO (karbon monoksida) merupakan gas yang tak berwarna, tak berasa, dan tak berbau. Ia terdiri dari satu atom yang kovelen yang berkaitana dengan satu atom oksigen. Dalam…
- Teori Kinetik Gas – Persamaan Umum Gas, Hukum Gas… Pernahkah Anda melihat gelembung-gelembung ketika minuman bersoda dituangkan? Bagaimana bentuk dan jumlahnya? Gelembung-gelembung minuman bersoda merupakan inti molekul-molekul. Gelembung-gelembung minuman bersoda akan berjumlah banyak dan volumenya semakin membesar saat dituangkan.…
- Pegertian Membran Sel Membran sel atau membran plasma adalah struktur selaput tipis yang menyelubungi sebuah sel yang membatasi keberadaan sebuah sel, sekaligus juga memelihara perbedaan-perbedaan pokok antara isi sel dengan lingkungannya. Namun membran sel tersebut tidak…
- Pengertian, Ciri-Ciri, Fungsi, Struktur dan Jenis… Pengertian, Ciri-Ciri, Fungsi, Struktur dan Jenis Pembuluh Darah Kapiler Lengkap – Pembuluh darah kapiler atau capillaris adalah pembuluh darah terkecil di tubuh dengan diameter 5-10 μm. Pembuluh darah ini menghubungkan arteriola…
- Rangkuman Materi Metabolisme dan Contoh Latihan Soal Lengkap Rangkuman Materi Metabolisme dan Contoh Latihan Soal Lengkap Bertemu lagi dengan postingan-postingan mengenai materi pelajaran sekolah, kali ini ini akan membahas rangkuman dari materi yang telah kita pelajari pada artikel…
- Makromolekul : Amina kali ini kami akan membahas materi kimia tentang amina pada makromolekul. Amina Amina ialah turunan amonia (satu atau lebih atom H disubstitusi). Amina bisa digolongkan menjadi : Amina primer, yaitu…
- Atom-atom dibawah ini yang paling lemah menarik… Atom-atom dibawah ini yang paling lemah menarik elektron adalah yang memiliki nomor atom . . . . A. 16 B. 13 C. 9 D. 7 E. 17 Jawaban : D.…



